糖尿病是一种多病因、多机制导致的,以慢性高血糖为特征的代谢性疾病。随着病程进展,胰岛β细胞功能衰竭,代谢紊乱进一步加重,出现糖尿病肾病(DN)、糖尿病视网膜病变(DR)、糖尿病足(DF)、糖尿病性神经源性膀胱等相关并发症。国际糖尿病联盟指出,如果没有更有效的干预措施,全球糖尿病患者预计2030年达到5. 78亿人,2045年将达到7亿人,其中2型糖尿病(T2DM)占比最高,达90%~95%。目前的治疗方式控制饮食、加强运动、口服降糖药物、胰岛素补充或替代治疗,都只能暂时保持血糖的相对稳定状态,而不能从根本上解决高血糖及长期高血糖引发的严重并发症。胰岛移植或可解决根本问题,但胰腺供体的有限来源及终身免疫排斥问题又是诊治过程中难以解决的障碍。而干细胞具有分化为产胰岛素细胞、改善胰腺再生和改善胰岛素抵抗的潜能,为治疗糖尿病提供了可能的发展方向[1]。目前干细胞治疗T2DM的动物和人体研究取得一定进展,各种干细胞来源不同其机制各异,间充质干细胞(MSCs)是研究最多的细胞,MSCs 治疗可能代表了优化T2DM血糖控制的新途径。
《Stem Cells Research& Therapy》期刊上刊登了一项关于MSCs治疗2型糖尿病患者的单中心随机双盲对照II期临床试验的结果[2]。结果显示,经静脉注射治疗后,MSCs可以降低对外源胰岛素的需要,减轻其对胰岛素的抗药性。对于2型糖尿病患者,脐带间充质干细胞是一种有潜力的疗法。

这项临床研究主要探讨脐带间充质干细胞(UC-MSCs)治疗中国成人2型糖尿病(T2DM)的有效性和安全性。在这项单中心、双盲、随机、安慰剂对照的II期临床试验中,91例患者被随机分为3组,分别静脉输注UC-MSCs (n= 45)或安慰剂(n=46),每4周间隔一次,从2015年10月至2018年12月,随访48周。主要终点是糖化血红蛋白(HbA1c)水平<7.0;48周时,每日胰岛素降低50%。次要终点是代谢控制、胰岛β细胞功能、胰岛素抵抗的改变和安全性。临床数据显示,在48周时,20%UC-MSCs组的患者和4.55%安慰剂组的患者达到主要终点(P < 0.05, 95%置信区间(CI) 2.25 28.66%)。UC-MSCs组胰岛素降低率明显高于安慰剂组(27.78% vs 15.62%,P < 0.05)。HbA1c水平下降1.31% (9.02±1.27% ~ 7.52± 1.07%,P < 0.01),安慰剂组仅为0.63% (8.89±1.11% ~ 8.19±1.02%,P>0.05;两组间P = 0.0081)。UC-MSCs组葡萄糖输注率(GIR)明显增加(从3.12 mg/min/kg增加到4.76 mg/min/kg, P< 0.01),而安慰剂组没有显著变化(从3.26到3.60 mg/min/kg, P>0.05; P< 0.01代表两组差异)。两组患者胰岛β细胞功能均无改善。未发生UC-MSCs移植相关重大的不良事件。总体来说,UC-MSCs移植可能是中国成人T2DM的一种潜在治疗方法。
UC-MSCs或安慰剂治疗后的胰岛素需求和HbA1c水平
糖尿病及相关并发症危害巨大,目前传统治疗效果有限,且价格昂贵。近年伴随干细胞的深入研究,利用干细胞治疗恢复胰岛功能为糖尿病患者带来新的希望[3]。其中 MSCs具备强力自我增殖、分化潜能、免疫调节等特点,且易于在体外分离和扩增,培育周期较短,免疫原性低,免疫排斥少,作为成体干细胞规避了伦理问题,使其成为细胞治疗的理想选择[4,5]。随着临床试验的深入,在临床上,干细胞在糖尿病的治疗上有很大的发展空间。
参考文献
[1] Malone JI, Hansen BC. Does obesity cause type 2 diabetes mellitus (T2DM)? Or is it the opposite? Pediatr Diabetes. 2019 Feb;20(1):5-9. doi: 10.1111/pedi.12787. Epub 2018 Nov 5. PMID: 30311716.
[2] Zang L, Li Y, Hao H, Liu J, Cheng Y, Li B, Yin Y, Zhang Q, Gao F, Wang H, Gu S, Li J, Lin F, Zhu Y, Tian G, Chen Y, Gu W, Du J, Chen K, Guo Q, Yang G, Pei Y, Yan W, Wang X, Meng J, Zhang S, Ba J, Lyu Z, Dou J, Han W, Mu Y. Efficacy and safety of umbilical cord-derived mesenchymal stem cells in Chinese adults with type 2 diabetes: a single-center, double-blinded, randomized, placebo-controlled phase II trial. Stem Cell Res Ther. 2022 May 3;13(1):180. doi: 10.1186/s13287-022-02848-6. PMID: 35505375; PMCID: PMC9066971.
[3] El-Badawy A, El-Badri N. Clinical Efficacy of Stem Cell Therapy for Diabetes Mellitus: A Meta-Analysis. PLoS One. 2016 Apr 13;11(4):e0151938. doi: 10.1371/journal.pone.0151938. PMID: 27073927; PMCID: PMC4830527.
[4] Kassem DH, Kamal MM. Therapeutic efficacy of umbilical cord-derived stem cells for diabetes mellitus: a meta-analysis study. Stem Cell Res Ther. 2020 Nov 16;11(1):484. doi: 10.1186/s13287-020-01996-x. PMID: 33198815; PMCID: PMC7667841.
[5] Li B, Cheng Y, Yin Y, Xue J, Yu S, Gao J, Liu J, Zang L, Mu Y. Reversion of early- and late-stage β-cell dedifferentiation by human umbilical cord-derived mesenchymal stem cells in type 2 diabetic mice. Cytotherapy. 2021 Jun;23(6):510-520. doi: 10.1016/j.jcyt.2021.01.005. Epub 2021 Mar 16. PMID: 33736932.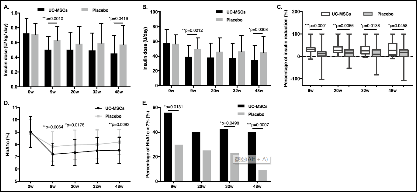
成都市武侯区一环路南一段24号四川大学科技创新中心405号
yhsw33399@163.com
028-85217799
